Isi
- tahap
- Metode 1 Menyeimbangkan persamaan dengan metode coba-coba
- Metode 2 Menyamakan persamaan dengan metode aljabar
Dalam kimia, persamaan menentukan apa yang terjadi selama reaksi kimia. Di sebelah kiri persamaan, kami menempatkan reagen yang digunakan untuk percobaan dan di sebelah kanan, produk yang diperoleh selama percobaan. Menurut prinsip konservasi massa (Lavoisier) selama reaksi kimia, tidak ada atom yang hilang, tidak ada yang dibuat, mereka bergabung secara berbeda. Singkatnya, Anda harus memiliki nomor data yang sama dari setiap elemen di sebelah kanan seperti di sebelah kiri persamaan. Itulah sebabnya persamaan keseimbangan harus selalu seimbang.
tahap
Metode 1 Menyeimbangkan persamaan dengan metode coba-coba
-
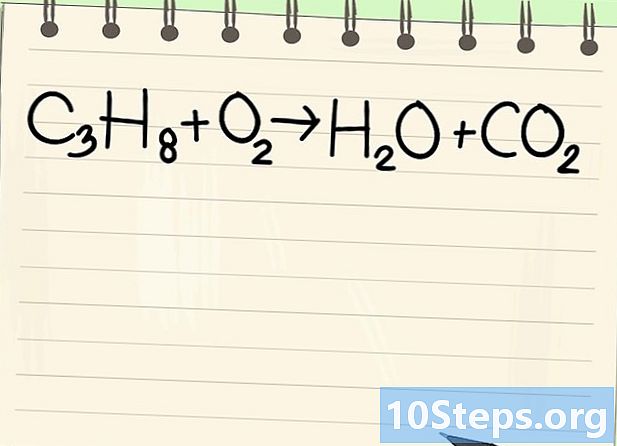
Perhatikan persamaan keseimbangan. Kami akan memperlakukan persamaan berikut:- C3H8 + O2 -> H2O + CO2
- Ini adalah persamaan pembakaran propana (C3H8) dalam oksigen: air dan karbon dioksida diperoleh.
-
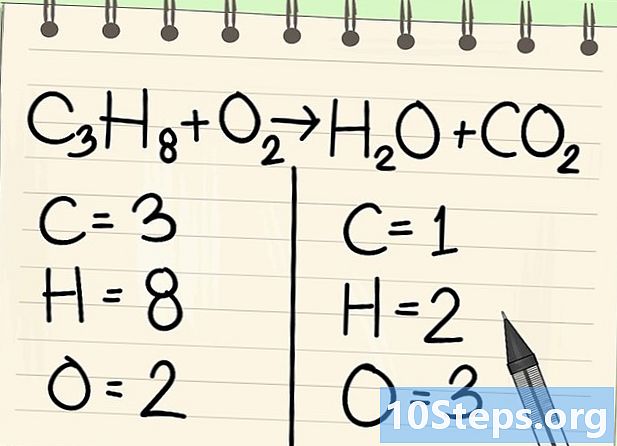
Hitung atomnya. Masukkan jumlah datom dari setiap elemen di satu sisi persamaan, lalu yang lain. Untuk ini, perhitungkan indeksnya, jika tidak ada, indeksnya adalah 1.- Di sebelah kiri, ada 3 atom karbon, 8 hidrogen dan 2 oksigen.
- Di sebelah kanan, ada 1 atom karbon, 2 hidrogen dan 3 oksigen.
-
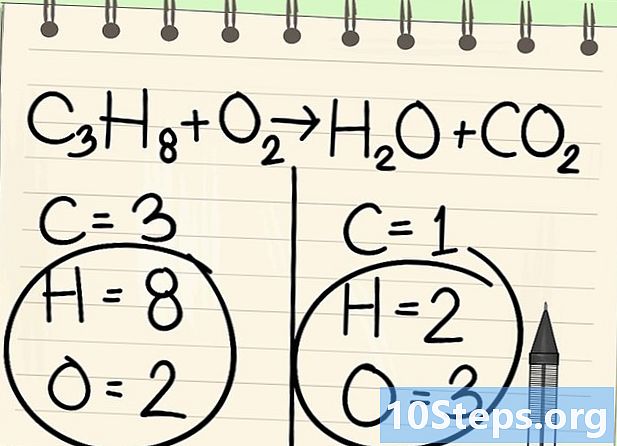
Singkirkan sebentar hidrogen dan oksigen. -

Mulailah menyeimbangkan dengan elemen yang tepat. Kami selalu memulai dengan yang ada dalam molekul sebelum dan sesudah reaksi. Jika ada beberapa, ambil satu yang monovalen di salah satu molekul. Di sini kita mulai dengan atom karbon. -

Seimbangkan atom karbon. Tambahkan, di sebelah kanan, koefisien ke molekul karbon dioksida (CO2) di mana karbon latom itu sendiri. Kami akan menempatkan 3 untuk mendapatkan 3 atom kiri.- C3H8 + O2 -> H2O + 3CO2
- Karenanya kami memiliki 3 atom karbon di sebelah kanan berkat koefisien (3CO2) dan 3 atom karbon di sebelah kiri berkat indeks (C3H8).
- Dalam sebuah persamaan, Anda bisa meletakkan semua koefisien yang Anda inginkan, tetapi Anda tidak bisa menyentuh petunjuknya.
-
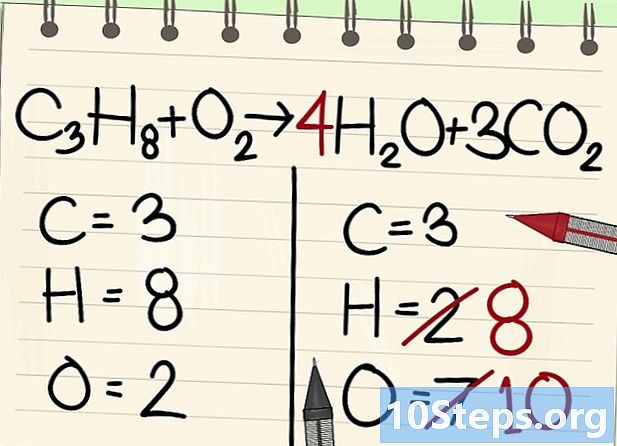
Seimbangkan atom hidrogen. Karena Anda memiliki 8 kiri persamaan, Anda perlu sebanyak kanan.- C3H8 + O2 --> 4H2O + 3CO2
- Di sebelah kanan, Anda akan meletakkan koefisien 4, karena hidrogen bivalen dalam molekul air: indeks 2 menunjukkan bahwa dua atom hidrogen terkait.
- Untuk mendapatkan jumlah atom hidrogen di sebelah kanan, Anda kalikan koefisien 4 dengan indeks 2, atau 8 atom.
- Adapun atom oksigen, di sebelah kanan, sekarang ada 6 di satu sisi, yang berasal dari tiga molekul 3CO2 (3 x 2 = 6 atom) dan 4 dari 4 molekul 4 H2O (4 x 1 = 4 atom), yaitu total 10 atom oksigen.
-
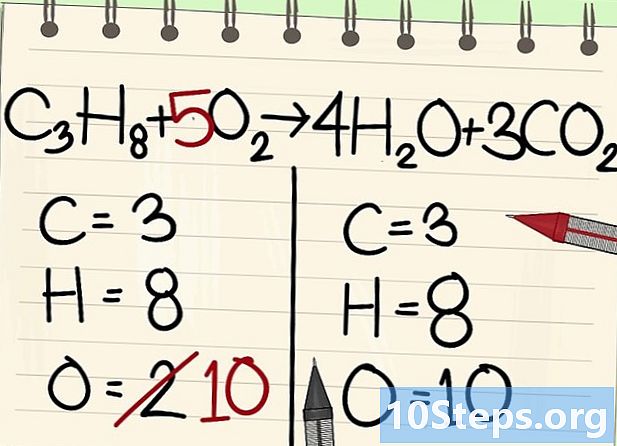
Seimbangkan atom oksigen.- Karena keseimbangan karbon dan hidrogen, jumlah atom oksigen tidak sama di kedua sisi persamaan. Kami melihat sebelumnya bahwa ada 10 atom oksigen di sebelah kanan (4 dari molekul air, dan 6 dari molekul karbon dioksida). Di sebelah kiri, hanya ada 2 (dari O2).
- Untuk menyeimbangkan oksigen, tambahkan koefisien 5 ke molekul oksigen kiri: Anda memiliki 10 atom oksigen di sebelah kiri dan yang lainnya di sebelah kanan.
- C3H8 + 5O2 -> 4H2O + 3CO2
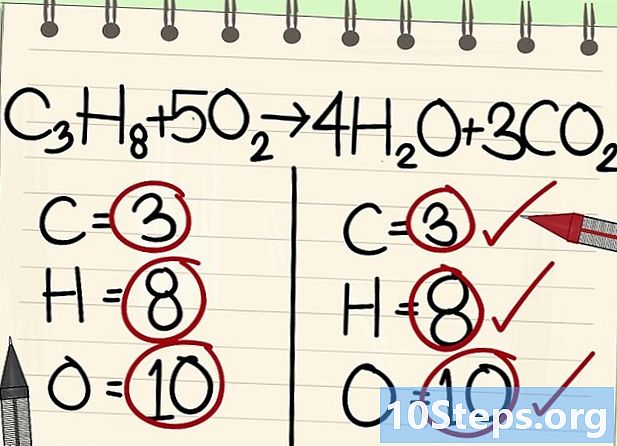
- Semua atom (karbon, hidrogen, dan oksigen) seimbang: persamaan Anda seimbang.
Metode 2 Menyamakan persamaan dengan metode aljabar
-

Tulis persamaannya untuk diseimbangkan. Tetapkan setiap molekul dengan koefisien literal. Kami akan memanggil mereka memiliki, b, c dan d. -
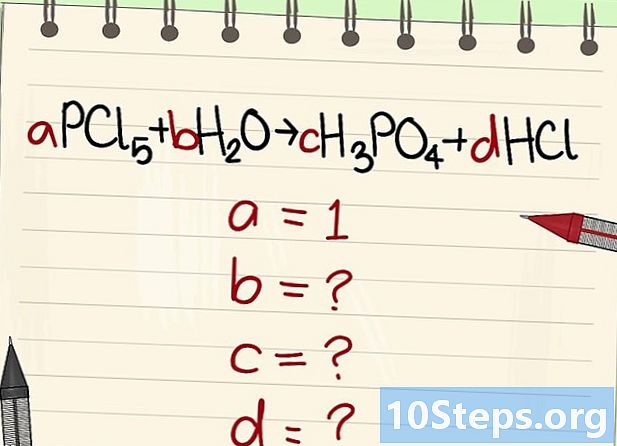
Temukan nilai dari koefisien literal lainnya. Kami akan menanyakan itu memiliki = 1. -

Temukan hubungan antara koefisien-koefisien ini. Melihat ke kiri (reagen) dan kanan (produk), membangun hubungan antara koefisien yang berbeda ini.- Ambil persamaan berikut: aPCl5 + bH2O = cH3PO4 + dHCl. Telah dinyatakan bahwa a = 1, yang berarti bahwa c = a, d = 5a dan 2b = 3c + d. Perhitungan dilakukan, c = 1, d = 5 dan b = 4.

- Ambil persamaan berikut: aPCl5 + bH2O = cH3PO4 + dHCl. Telah dinyatakan bahwa a = 1, yang berarti bahwa c = a, d = 5a dan 2b = 3c + d. Perhitungan dilakukan, c = 1, d = 5 dan b = 4.